- 論文全文:Comprehensive Thione-Derived Perylene Diimides and Their Bio-Conjugation for Simultaneous Imaging, Tracking, and Targeted Photodynamic Therapy於2022年9月7日發表於《JACS》:https://pubs.acs.org/doi/full/10.1021/jacs.2c07967
- 作者名單:Yao-Lin Lee, Yi-Te Chou, Bo-Kang Su, Chi-chi Wu, Chih-Hsing Wang, Kai-Hsing Chang, Ja-an Cnnie Ho*, and Pi-Tai Chou*
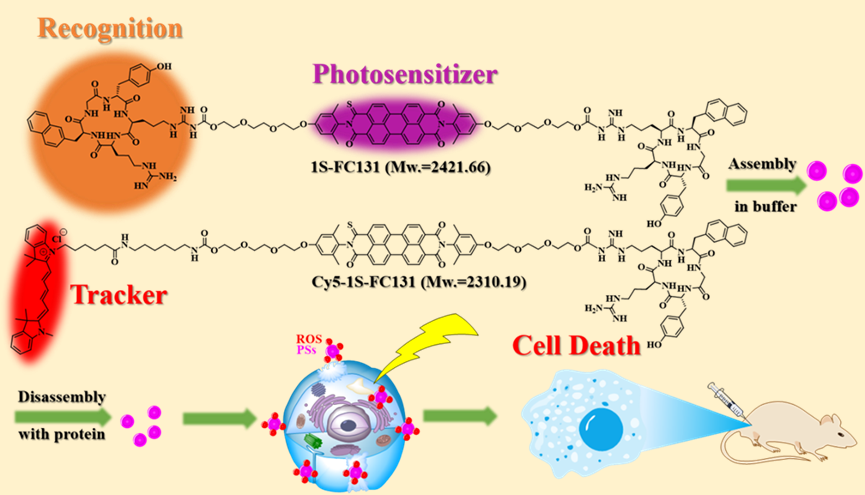
在癌症治療上,光動力療法因其非侵入性、時空間選擇性與低廉成本而廣受研究者青睞,但美中不足的是光穿透度過淺、對氧氣依賴程度高與癌細胞選擇性低等因素讓光動力療法尚未被更廣泛地應用於癌症治療。本系周必泰教授與合聘教師何佳安教授(台大生技系)合作,設計出新穎的非重金屬光動力療法藥物:以雙光子吸收度高的苯苝二酰亞胺(3,4,9,10-perylenetetracarboxylic diimide)為主體,經過硫化反應得到一至四取代的產物命名為1S-PDI-D, 2S-cis-PDI-D, 2S-trans-PDI-D, 3S-PDI-D 和 4S-PDI-D (分別含1-4 個硫)。在測定這個系列的光物理性質後,發現其最低吸收(S0 → S2 (ππ*))會隨著硫取代數上升而紅移,且其單重態氧產率呈現了1S-PDI-D (~100%) > 2S-cis-PDI-D > 2S-trans-PDI-D >> 3S-PDI-D = 4S-PDI-D (~ 0%)的趨勢。透過理論計算得知這系列分子的三重態能量排序為1S-PDI-D (1.10 eV) > 2S-cis-PDI-D (0.98 eV) ~ 2S-trans-PDI-D (0.98 eV) > 3S-PDI-D (0.87 eV) > 4S-PDI-D (0.77 eV);由於1S-PDI-D的三重態遠高於單氧能階 (1Δg, 0.97eV),故可以做為一絕佳的光敏劑。根據這個發現,周老師與何老師的研究團隊設計了兩樣新藥物:1S-FC131為將1S-PDI-D分子兩端鏈接上具有癌細胞選擇性的FC131基團、而Cy5-1S-FC131是將1S-PDI-D分子一端連接FC131、另一端接具有螢光顯影的cyanine。細胞實驗證實1S-FC131和Cy5-1S-FC131均具有靶向性,可成功辨識人類非小細胞肺癌細胞(A549),但卻不會識別本研究中其他三種受測的正常肺細胞。此外,1S-FC131和Cy5-1S-FC131皆具備光動力治療功能。動物實驗亦證明,1S-FC131和Cy5-1S-FC131在異位異種移植的A549肺癌小鼠模式中表現出色的抗腫瘤能力,其中Cy5-1S-FC131具有同步螢光追踪及靶向光動力治療的優勢。Cy5-1S-FC131的靶向性、療效和成像功能使之具有潛力成為腫瘤精準醫學中十分有前景的治療型探針。本研究成果已發表在化學領域頂尖期刊美國化學會志(Journal of the American Chemical Society)。