作者: Mark Peplow
原始文章: Nature 2015, 525, 18-21.
譯者: 蔡蘊明
(本譯文特商請台灣大學化學系的邱勝賢、楊吉水、與李弘文三位教授提供圖片,並幫忙校閱,特此致謝)
受到生物的啟發,化學家們創造出一系列精彩的分子元件,可做為開關、馬達、以及棘輪,
現在是將它們用來做一些有用的事情的時候了。
機器人在它的軌道上緩步移動,定期的停下來並伸出臂膀小心的拿起一個零件,臂膀將這個零件連接到機器人背上的一個精巧的裝置上,接著,機器人往前繼續行進並重複上述的動作-系統化的將零件們按照設計圖樣準確的組裝起來。
這可能是一個高科技工廠裡的一幕情景-只不過這個組裝線才僅有幾個奈米的長度,零件們是一些胺基酸,產品是一個小的胜肽,而機器人則是英國曼徹斯特大學的化學家 David Leigh 所創造的,那是有史以來所製造過最複雜的分子尺度的機器之一。
這並非一個寂寞的路程,Leigh是屬於現在正在成長的一群分子建築師之一,他們受到啟發而企圖模擬細胞中發現之類似分子機器的生物分子-致動蛋白(kinesin),它可以在細胞中的微小腳架上行進;或核醣體,於其上透過基因密碼的讀取來製造蛋白質。在過去的25年中,這些研究工作者設計了一系列令人印象深刻的開關、棘輪(防倒轉)、馬達、桿子、環、螺旋槳、以及更多的-分子機械裝置,好似奈米尺度的樂高積木般能組裝起來。由於分析化學工具的進步,以及為了合成複雜的有機化學分子所研發的許多化學反應,使得這個領域的發展正在加速中。
現在這個領域已到了一個轉捩點,荷蘭格羅寧根大學(Groningen University)的化學家 Ben Feringa 說“我們已經做出了50到60多個不同的馬達,但現在製造更多的馬達已經不若如何真正運用它們那麼吸引我了”。
今年五月(2015年),在一個極具影響力的美國戈登會議(Gordon conferences)中,上述的論點已經清楚的被聽到。這是第一次的在此會議中有一個組群聚焦在分子機器以及其運用的課題上,該會議的主辦者,以色列雷霍沃特(Rehovot)的魏茨曼科學研究所(Weizmann Institute of Science)的化學家 Rafal Klajn 認為這是極為明顯的徵兆,宣告這個領域的時代已經到來。Leigh 指出“在十五年內,我認為它將成為化學以及材料設計中的一個核心部分”
要到達那個階段將不容易,研究人員需要學習如何讓上億的分子機器協同的運作而產生可量度的巨觀現象,例如改變一個材料的形狀而讓它如同一個人工肌肉般運作。他們也需要讓這些機器易於控制,並確保它們能執行無數次的運作而無損壞。
這是為何許多這個領域的工作者並不預期初期的運用能涉及複雜的裝置,不過他們預測那些基礎的分子機器之零件將可運用在各種不同的科學領域中:像是光啟動的開關用來釋放標靶藥物;或製成能儲存能量或能呼應光線而膨脹收縮的聰明材料。Klajn 認為那意味著分子建築師們需要聯繫那些能從這些分子機器的零件得到幫助的研究工作者“我們需要說服他們這些分子的確是很精彩的”。
梭具的啟用
回朔許多現今的分子機器之源頭,那是 1991年的一位化學家 Fraser Stoddart (現在美國西北大學)所製造的一個相當簡單的裝置,該裝置被稱為輪烷(rotaxane),於其中,一個環狀的分子套在一個〝軸〞上,那是一個直線型的分子,兩端各裝有一個巨大的塞子使得環不會脫落。在這個特殊的軸上,分在兩邊,有兩個化學官能基團,二者皆能與環狀的分子結合(圖一)。Stoddart 發現那個環可以在這兩個位置上來回跳動,是而製造出第一個分子梭(molecular shuttle)。
到了 1994 年,Stoddart 將其設計做了改進,軸上面具有兩個不同的結合位置,分子梭存在於溶液中,當改變溶液的酸度時就可強迫環從一個位置跳到另一個位置,這就讓此分子梭變成為一個可以反覆切換的開關。類似的分子開關有一天可能被用做感應器,能偵測熱、光、或特定的化學品,又或可用來控制一個奈米容器,在容器到達人體內正確的位置以及正確的時間點打開艙門,將化學藥物分子的貨物送出。
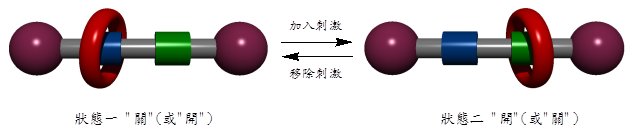
圖一 在輪烷溶液中引入外加刺激(如酸度的改變),可驅使內鎖大環從藍色的辨識中心移動到綠色的辨識中心上。而移除此外加刺激後,大環又會回到原先圍繞藍色辨識中心的狀態。兩種狀態可受操控的相互轉換,好似一個開關裝置一般。(本圖由台灣大學化學系邱勝賢教授提供)
Stoddart 的機器展現出的兩種性質,在之後所發展出的分子機器當中不斷出現。首先,環與軸在結合處的連結,並非原子之間結合形成分子的那種強的共價鍵,相反的,那是透過前述的兩個部分所具有的部分電荷之間的微弱靜電引力來維繫,這使得相互的連結容易生成但也易破壞,就好像是兩股DNA 之間透過氫鍵形成的拉鍊一般,可輕易的關上或打開。其次,梭子不需要外部的能量來將之拉來拉去,它僅僅是透過在溶液中與其它分子的碰撞來推動,這種撞擊的行為稱為布朗運動(Brownian motion)。
許多其它的開關很快的發展了出來,有些是透過光或是溫度的改變來控制,另有些是透過與溶液中特定的離子或分子結合來運作,很像是細胞膜上離子通道的機制,透過化學的訊號來開啟或關閉。
不過 Stoddart 又將他的研究帶往了另一個方向,他與在美國加州理工學院的 James Heath 合作,用上百萬個的輪烷製成一個記憶體,那些輪烷夾在矽與鈦電極之間,透過兩個狀態之間的切換來記憶數據,這個分子算盤約具13 微米(10-6 m)的長寬,含有 160,000 位元,每一個位元是由數百個輪烷所構成 – 其密度大約是每平方公分100 GB (gigabits,十億位元),這與現今商業上最好的硬碟可以相提並論。
用了二十四個表現最好的位元,Stoddart 實驗小組人員展示可將 ”CIT” 三個字母(代表加州理工學院)儲存和取出,只不過這些開關並不堅固,通常使用不到一百次就會壞掉。一個有潛力的解決方案是將它們放入一種稱為金屬有機骨架(MOF, metal-organic frameworks)當中,MOF是堅固而具有孔洞的晶體,它能保護開關,並將開關有秩序的安排成一個三度空間的陣列。
今年初,在加拿大溫莎大學(University of Winsor)的Robert Schurko與Stephen Loeb,展示他們能在每一立方公分的MOF 當中將約 1021 個分子梭裝入;而上個月Stoddart 公佈了另一種內含可開關型輪烷的 MOF,裝在一個電極上,而其中的輪烷可透過電壓的改變一起切換開關。
這些MOF研究工作者,希望這種三維固體支架能比傳統矽的電晶體提供更高的密度,而且能讓這些分子較易控制,最終具有大量數據儲存的潛力,Loeb說“用科幻小說的方式來想,要做到讓一個分子來作為一個位元”,不過他覺得較實際的來看,一小粒內含數百個開關的MOF,可用作一個位元,只要那粒中大部分的開關都運作正常,它們將可集體成為可信賴的數碼。
另有其他的研究者用輪烷作為可切換的催化劑。在2012年,Leigh 報導了一個系統,在其輪烷的軸上有一個氮原子,通常它是與環結合的,當加入酸,環就會移到一邊去而將氮原子暴露出來以催化一個常見的化學反應。更進一步的,去年十一月Leigh發表了一個輪烷的系統,其中有兩個催化的位置,將環從一個位置移到另一個位置,化學家可以切換輪烷的活性,使得兩種化學反應可以依序發生。Leigh現在正企圖將好幾種不同的可開關催化劑放在同一溶液中,透過一系列的開關訊號將分子依序結合,生成複雜的結構,就很像細胞中眾多的酵素所做的事一般。
奈米馬達
在1999年,於分子梭和開關的初步實驗成功之後,這個領域又向前跨越了一大步而創造出了第一個人工合成的分子馬達,那是Feringa的研究小組所製造的,這個裝置是一個單一分子,上面具有兩個相同的〝槳〞的單元,相互透過一個碳-碳雙鍵連結,這使得兩個槳是固定住的,但當一束光將雙鍵破壞成為單鍵時,槳就可以開始旋轉了(見圖二的例子),重要的是受到槳的形狀限制,只能往一個方向轉動 – 而只要持續的提供光和一些熱,這個馬達即可持續的轉動。
Feringa 更進一步,用類似的馬達創造了一個四輪轉動的〝奈米車〞。他也展示了這種馬達能給予液晶足夠的扭力,將其上的一個玻璃棒慢慢的旋轉,那個棒子有28 微米長 – 是馬達的好幾千倍大。
有些化學家批評這些馬達,認為它們雖然很可愛,但終究沒甚麼用處。一位在德國慕尼黑的 Luwig Maximilian 大學的化學家Dirk Trauner說“我一直對這種人造馬達有點疑慮 – 它們太難合成,也太難放大製程”。
不論如何,在其背後運作的化學原理的確是非常有用的,運用相同的光驅動機制。研究工作者已經開發出100種類似藥物的化合物,可以透過光來開啟或關掉其活性。
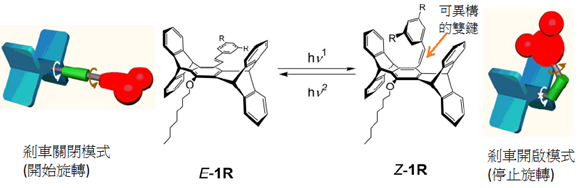
圖二 這是一個台灣大學化學系楊吉水教授設計的轉輪體系,其中有一個可以透過光異構化的碳-碳雙鍵(卡通圖中的綠色部分),在左邊的E-1R分子結構中雙鍵兩端的取代基相互遠離,旋轉是被允許的,但透過光的照射,可將雙鍵異構化成為Z-1R的結構,此時雙鍵兩端的取代基相互接近,紅色的結構會卡在兩片藍色扇葉之間,好似剎車一般,此時無法旋轉,透過另一道頻率(n)不同的光又可將雙鍵異構成E-1R,等於將剎車關閉,又可旋轉了。(本圖由楊吉水教授提供)
例如在七月份,由Trauner所領導的研究小組發表了一個藥物,是combretastatin A-4 (康普瑞汀)的光開啟版本,康普瑞汀具有很高的抗癌藥效但也有嚴重的副作用,因為它不但會攻擊腫瘤細胞但是也會攻擊健康的細胞,該研究小組所開發的這種可開關的藥,能大幅度降低系統性的副作用:此藥的結構具有一個氮-氮雙鍵,讓其上的兩個結構單元固定在相互遠離的位置,此時沒有藥物活性,只有在照射藍光時,雙鍵破壞成為單鍵後(暫時性的激發態,釋放能量則回到雙鍵),兩個結構單元就可藉旋轉改變位置成為有藥效的結構型態。Trauner指出,可以透過一個可彎曲的管子,或移植手術用的裝置,將該藥物引入一個只有10 微米寬度的組織區域,Trauner 正計畫進行老鼠身上的實驗來測試此化合物對癌症的療效。
他也希望運用這種利用光開啟的化合物,來恢復黃斑點退化症(macular degeneration)或網膜色素沉著症(retinitis pigmentosa)病患的視力,這類的病是源自於眼睛感光的桿細胞以及錐狀細胞的損壞,他說“那根本是伸手可採的果實 – 因為是在眼睛,我們不需要去擔心如何將光引入”。去年他展示了將一個稱為DENAQ的光啟動分子,對盲鼠眼睛進行一次的注射即可恢復其部分的視力,能區別明暗並維持好幾天。該研究小組目前正在進行靈長類動物的藥物測試,並希望能在兩年內開始人體實驗。
Trauner與Klajn都同意,主要的挑戰將會是說服謹慎的製藥界,體認光啟動藥物是具有潛力的,即便沒有任何在人體上使用的先例,Trauner說“我們需要讓製藥界對光藥學感到興奮,一旦看到其價值,我們就有機會了”。
沿路行走
早在任何物種進化到能在陸地上行動之前,細胞就已經在運用腳來作為其機器,主要的例子就是一類具有雙叉的蛋白質,稱為致動蛋白(kinesins),當它們攜帶著貨物行走在細胞中微管構成的堅硬腳架上,以達到朝特定方向的運輸功用時,一〝腳〞放在另一〝腳〞之前。
受到致動蛋白的啟發,研究人員利用DNA製造了人工的行走器(參考圖三的例子),這類的分子通常有兩隻腳,分別固定在兩股互補的DNA所鋪的路軌上,當加入另一可以競爭的單股DNA時,就可以釋放一隻腳,讓行走器向前跨出一步。一個非常突出的例子是在2010年紐約大學的Nadrian Seeman所發表的系統,他的DNA行走器共有四隻〝腳〞和三隻〝手〞,它能攜帶著金奈米顆粒在折疊的DNA所鋪成的地磚上行走。
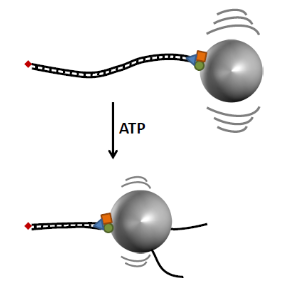
圖三 DNA解旋酵素是另一個自然界的DNA行走器,可藉由轉換ATP水解所產生的能量,行走在DNA上,進而達到將DNA的雙股解旋。本圖中藍色三角的部分具辨識DNA序列的功能,方形與圓形的部份,分跨在DNA的兩股上面行走,台灣大學化學系李弘文教授的研究顯示方形與圓形的部份能各自走在DNA的單股上,達成解旋雙股的目的。(本圖由李弘文教授提供)
和細胞中具方向性的行走器相比,對DNA行走器來說 – 以及迅速的從其它實驗室研製出的變體 – 除非設計一個內建的棘輪來阻止它往後方跨步,否則將漫無目的的遊蕩著。在許多的行走器中,棘輪控制的關鍵是在於與腳黏合和釋放相關的化學反應之相對速率,並藉著布朗運動,推動釋放開的腳向前走動。
在過去的這幾年,仔細的化學研究與分子動力模擬,顯示這種〝布朗棘輪〞的概念是所有化學推動的分子機器背後的基礎,這包括了許多生物馬達。例如在2013年,位於美國安納保的密西根大學,由Nils Walter所領導的研究小組發現同樣的機制運作於剪接體(spliceosome),那是一個細胞的機器,用來從RNA上剪下一部份,然後將其上的基因資訊轉譯以製備蛋白質,Walter說“致動蛋白用它,核醣體用它,而且剪接體也用它”。
既然同樣的原理在生物機器與合成分子機器的背後運作,因此這兩個領域的研究工作者應該可以相互分享知識,Walter說“一般而言,它們現在是相隔很遠的領域,我認為如果大家能圍著同一張桌子來討論時,將導致下一輪的突破”。
火箭科學
同時,受到1966年為影迷推崇的影片〝聯合縮小軍(Fantastic Voage,又翻成神奇旅程)〞之中縮小版潛水艇的啟發,化學家也創造了一系列微米大小的顆粒和管子,它們能像火箭般穿射過液體。
這類的馬達中有些攜帶了一種催化劑,能從周遭的液體 – 通常是過氧化氫 – 製造出一連串氣泡而產生衝力;另有一些則是透過光或外界的電場或磁場直接取得動力,用來行駛其船艦。在加州大學聖地牙哥分校(UCSD)的奈米工程學家Joseph Wang說“這些奈米馬達每秒可行進其長度一千倍的距離,真難以置信”,他認為最有潛力的運用是在快速藥物投遞,或低價格的環境汙染清潔器 – 雖然許多此領域的學者提醒大家,現在說奈米馬達將會把傳統的方法擊潰仍嫌過早。
過氧化氫是個很強的氧化劑,很難適於細胞內使用,Wang承認“當所有的工作都只是基於過氧化氫,的確有許多的懷疑”,但是在去年的十二月,他發表了一個微型馬達,適用於活的動物身上,那是由一個約20 微米長的塑膠管子做成的,內含一個鋅金屬核心,能與胃酸反應,產生具推動力的氫氣泡。
這些管子安全的在一隻老鼠的胃中四處穿梭了十分鐘,Wang利用它們攜帶一些金奈米顆粒進入附近的胃部組織;僅施予簡單的奈米顆粒之老鼠胃壁上,與用奈米管投藥的方法比較,最終只能附上少三倍的金。
Wang認為將藥物或顯影試劑負載在這種火箭上,能將之迅速而有效的投遞進入胃部組織當中,他說〝在未來五年內我們將會進展到實際的活體運用上,那將會是一個真正的神奇旅程〞。
現在這些火箭和分子機器的研究之間的交集仍有限,Klajn說“但我們能帶來很多的機會”,例如他指出,將一個微型馬達表面塗佈上光啟動的開關,可提供其行動的額外控制力。
抽取出來
製造真正有用的分子機器的追尋當中,研究工作者正開始將不同的零件整合成一個單一的裝置,今年五月份,Stoddart發表了一個人工分子幫浦,能將溶液中的兩個環形分子拉入一條儲存鏈上,每一個環滑過在鏈子一端的塞子,吸引到一個可以切換的結合點(開關處),切換一下那個開關可將環推過下一個路上的障礙而到達一個儲存區。
這個系統無法抽取其它型態的分子,而且需要透過許多錯誤嘗試才能製造出,Stoddart嘆了口氣說“那是一個漫長的路程”,但是這證明了分子機器可以用來濃縮分子,將一個化學系統推離平衡點,就好像生物系統製造一個位能儲存狀態時,刻意的移動離子或分子以產生一個濃度的梯度一般,他說“我們正在學習如何的製造一個能量的棘輪〞。
Stoddart指出這些發展能讓這領域往兩個主要的方向來演進:停留在奈米,給予這些分子機器用其它的方法做不到的奈米尺度的工作;或走向大尺度,用上億的奈米機器合力改造材料或移動大量的貨物,就好像一群螞蟻軍隊般運作。
或許一個奈米尺度的原始例子是Leigh 的分子組裝線,受到核醣體的啟發,它是基於一個輪烷系統,沿著一個軸將胺基酸抓起,接著到一個正在成長的胜肽鏈上。但是這個裝置也可能具有大尺度的運用性,在36小時之中,1016 個機器合力能製造出幾個毫克的胜肽,Leigh說“雖然它無法做到在實驗室裡半小時能做到的事,但是這展示了你能有一個機器,可沿著一條軌道,拿起一些分子建材並將它們組裝起來〞。Leigh正在研發另一種版本的機器,企圖製造有順序的聚合物,並具有特製化的材料性質。
相反的,上億分子機器的合作,能改變一個材料的巨觀性質。例如,能呼應光或化學分子而膨脹或收縮的凝膠,能做為可調整的鏡片或感應器,Feringa說“我打賭在未來五年內,你將有機會用到含有開關的聰明材料〞。
現在以已經開始看到輪烷類的分子的商業運用,在2012年宣佈的Nissan Scratch Shield 的iPhone外殼,是基於東京大學Kahzo Ito的研究,這個系統具有許多連接成8字型的一對對桶狀環糊精分子,聚合物的鏈子分別穿過8字的兩孔(各穿一股),當壓力施加在尋常的聚合物塗膜時,聚合物股鏈之間的連結會被破壞,但是8字形的一對環糊精分子可扮演滑輪系統的輪子,由於具有許多這種可移動的8字形滑輪交連位置,使聚合物的交連股鏈相互滑動而不會分離並紓解張力,這層膜甚至於能保護易碎的螢幕,不被槌子的敲擊而破壞。
對Stoddart而言,這顯示分子建築家們所開發的零件已經成熟到實用階段了,Stoddart說“這個領域走了很長的一條路,現在我們開始展示它是有用的〞。
譯者後記
這是最近 Nature 期刊上的一份特寫文章,簡介新穎分子機器之研究發展,剛好譯者本學期正在教醫學、牙醫、與電機系的普通化學課,而這篇特寫剛好在介紹化學、醫學、與工程的結合,一時興起,決定將此文翻譯成中文,做為學生的參考資料,該文所列之參考文獻就不再重複拷貝,有興趣的學子可回到原文尋找該文引述的文獻資料。其實在這個方向上,台灣大學化學系的邱勝賢教授就在研究奈米級分子電子元件之設計與建構;李弘文教授在研究巨大生物分子行走的機制;楊吉水教授在研究光化學與電化學控制之分子開關和分子機械,包括文中所提的分子螺旋槳,這些老師研究的課題均與本文章相關,因而特別邀請他們三位提供相關介紹圖片,讓這篇譯文有一點在地的味道。由於我沒有使用原文的圖說,有興趣者請參考原著。此外文中未能提及而為台灣大學化學系老師所專精的,包括彭旭明院士研究的奈米導線,陳逸聰教授鑽研的奈米材料與元件和生物感測器等等。對於這些領域有興趣的青年學子亦可進入上述教授的研究室網頁,一窺究竟,當然更歡迎選擇化學系,加入他們的實驗室,親身參與現今的尖端研究。
(蔡蘊明謹誌於台大化學系,2015/10/2)