藉本文向在臺灣推廣永續化學教育多年的尖兵劉廣定教授致敬
蔡蘊明於臺大化學系(2013/12/03)
化學是最為貼近人類生活的學問,它雖是組成物質的基礎,其運作存在於各處卻不易發現,因此人們常忘記自身的存在靠得就是化學。理想上,人類若能夠完全掌握化學,就生命而言,化學將能解決疾病與老化的問題;就生存而言,化學將能解決飲水,糧食和能源的問題。隨著科技進步帶來的舒適,人類無盡的追求更高的享受,背後支撐著的有很大一塊來自於化學,但是我們必須清楚的瞭解,目前能量的主要來源,在於將化學能轉換成為電能。很不幸的,這導致了大量二氧化碳的排放,許多人認為這造成地球氣候型態的改變,因此近年巨大的天災頻傳,造成大量生命財產的損失。人類追求物質的享受,需要新的物質,提供新的功能,但是我們不能忘記,那些新的物質都是靠著化學方法來合成的,多少的大自然資源被消耗?多少的廢棄物質因此流入河川,埋進土壤,排放至大氣?人類追求食物的享受,為了速成,使用了各種藥劑和添加物,來幫助動植物的生長,和加速食物的製造與處理,在這裡化學品的運用也扮演了重要的角色,台灣人近年來對此尤其是心有戚戚焉。每每當問題發生時,化學永遠是帶罪的羔羊,其實人類的無知和欲求才是罪惡之始。上述的誤解,甚至於被台灣的一支著名廣告利用,在電視上宣稱某某工坊痛恨化學。筆者在課堂上則藉機告訴學生,如果你/妳痛恨化學,那就等同於痛恨生命,因為生命的根基就在於化學。
綠色化學的十二原則
化學固然是無辜的,但是要解決人類製造的危機,仍需要使用化學的方法。在進入二十一世紀之前,就有一批化學家開始鼓吹綠色化學的概念,其中最著名者為阿那斯特斯(Anastas)與華納(Warner)所提出的綠色化學十二原則,受到化學界廣泛的重視。在臺灣大學化學系的劉廣定教授,最早在臺灣推廣綠色化學的概念,認為必須將此概念透過教育植入民心,可惜曲高和寡效果有限。為了呼應劉廣定教授的努力,特此為文,依照綠色化學的十二原則來看化學未來應依循的走向,希望台灣中等科學教育的工作者共同努力。劉廣定教授認為“綠色”的用詞過於偏狹,他覺得“永續(sustainable)”較為恰當,但是因為“綠色”較為直接,本文仍採用綠色化學來說明。
由於綠色化學十二原則內容有些複雜,英國諾丁漢大學 (The University of Nottingham) 的 Tang、Smith 和 Poliakoff 提出了 ”PRODUCTIVELY” 這十二個英文字母組成的單字,來幫助我們記得這十二原則[註],此單字中每一個字母,代表一個原則,筆者也東施效顰,提出十二個中文字來代表:
「廢物低、保降能、再簡化、可監危」
與此十二字相對應的是:
「防廢、物盡、低毒、保安、降輔、節能、再生、簡潔、催化、可解、監測、思危 」
等十二個辭,以下針對這十二個原則做較詳細的說明。
防廢(P)
防範勝於治療,這個原則就是在設計化學製程的時候,或是有選擇的時候,要避免產生廢棄物,或採用產生最少廢棄物的方法。化學反應的產物,除了製造的標的物質之外,也常會有隨伴的副產物產生,如果副產物沒有利用價值,就成為廢棄物,也就產生後續處理廢棄物的問題。以圖1為例,讓我們來比較一個簡單的氧化反應:將1-苯基乙醇氧化成為苯乙酮。方法一運用具有毒性的鉻金屬化合物為氧化劑,此法需要用當量級的試劑,也就是說,要氧化三莫耳的1-苯基乙醇,需要用到兩莫耳的三氧化鉻,而且還需要用掉三莫耳的硫酸,除此之外產生了一莫耳的硫酸鉻,和六莫耳的水。當然水不被視為廢棄物,但是硫酸鉻是具有毒性的重金屬之鹽類化合物,不可隨意丟棄,增加了處理的費用。與方法二相比,用空氣裡的氧氣為試劑,藉著少量催化劑的幫助,亦可達到同樣的目的,但是沒有其它的廢棄物,二者的優劣非常明確。
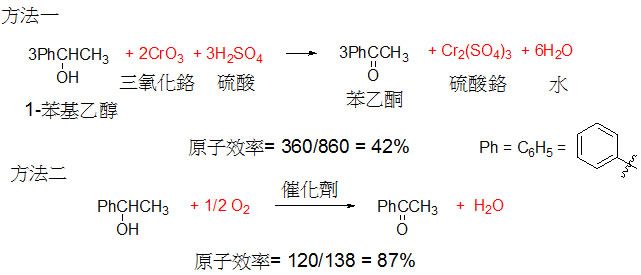
圖1 將1-苯基乙醇氧化成為苯乙酮的兩種方法:方法一運用兩當量具有毒性的三氧化鉻,以及三當量的硫酸為試劑,產生三分之一當量的硫酸鉻和六當量的水;方法二則是利用催化劑的幫助,以氧氣來進行氧化,除了苯乙酮只另產生水。
類似方法一這種型態的化學反應,早年製造了許多廢棄物,排放到環境中所造成的污染,導致日後需要花費大量人力物力去整治,得不償失。所幸先進國家現在很注重這個問題,制訂了許多的律法來防堵問題的出現,但是在落後或法治不彰的國家,仍然是嚴重的問題。
物盡(E)
這個原則是物盡其用之意,當我們設計反應時,應盡量朝著將所有起始物都轉變成有用的產物為目標。著名的化學家綽斯特(Trost)提出了有趣的原子經濟理論(atom economy),從一個平衡反應式,可輕易的按下式計算出其原子效率:
原子效率=(有用產物的總質量/所有起始物的總質量)x100%
以圖1的例子來看,方法一若由三莫耳的1-苯基乙醇(分子量 = 122)與兩莫耳的三氧化鉻和三莫耳的硫酸反應,這三種起始物總質量為860 克,得到的目標產物是三莫耳苯乙酮(分子量 = 120),總質量為360 克,代表此反應的原子效率為42%;按照這個方法計算,方法二的原子效率為87%。二者相比,方法二只損失17%的總原子質量,顯然是較佳的選擇。若是能找到適當的催化劑,只是脫去1-苯基乙醇中一當量的氫氣(H2) (圖2),即可得到苯乙酮,那原子效率更可高達98%。實際上氫氣也是有用的商品,那這種作法就成為100%的原子效率了。
物盡其用的原則只是一種精神,提供思考的方向,另外還有溶劑的使用,和能量的消耗,材料的價格和物質的毒性等等,需要考慮,最後做整體的決定(見後面的討論)。

圖2 將1-苯基乙醇直接脫氫氣得到苯乙酮
低毒(L)
這項原則是很明顯的,當我們選擇時,應盡量使用對人類和環境毒性最低的起始原料,產生的物質亦若是,上述圖1就是很好的例子。或許讀者會問,為何不以無毒為目標?但事實是,所有的化學物質過量都會產生問題,例如鹽巴(氯化鈉)吃太多,會因高血壓而亡,最近社會更發生了用鹽殺嬰事件;水喝太多,也會因為電解質流失太多而出問題;糖吃太多,易造成肥胖,而肥胖是許多疾病的危險因子,這是為何較實際的使用低毒的概念。
進一步的來看,這項原則應該擴大解釋為選用低危險性製程。我們應該將易燃性,爆炸性,以及在環境中被代謝的能力來考慮。我們不該消極的去使用,然後盡量減少接觸,和加強安全措施。真正應該從根本來做,想法減量或不用危險物質。
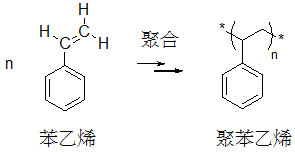
圖3 從苯乙烯可製備聚苯乙烯
另舉一例來看實際的運用典範:聚苯乙烯(圖3)是日常生活上很常用的聚合物,有許多的相關成品用做泡棉型態的包裝材料,其製作需要在冷卻成型時,運用發泡劑(blowing agent)混入。早期的發泡劑多使用氟氯碳化物(CFCs)等氣體,或揮發性高的有機溶劑,吹入使用。我們現在瞭解氟氯碳化物是造成地球臭氧層破洞的原凶;有機溶劑易燃而有潛在危險,且揮發出來對人體可能有害。針對這個問題,美國陶氏化學公司(Dow Chemical Company)發展了利用二氧化碳為發泡劑的方法,到了1996年該公司已經有七項相關專利在市面上,據估計這項科技的使用,每年成功為地球減少三百五十萬磅的氟氯碳化物或氫氯氟碳化物(HCFCs)。
保安(U)
簡單的說,本原則就是設計安全的化合物。化學產品的設計,應該以保持其功能而降低其毒性為原則。有關此點,現今藥物合成的研發是絕佳的例子。一個成功的藥,必須能治療疾病但卻不能具有毒性。化學結構與其功能是息息相關的,化學家具有很好的合成能力,可以透過結構的改變,來調整化合物的性質,例如增加某化合物的水溶性或疏水性。透過結構活性關係(SAR; structure-activity relationship)的研究來調整藥效,是現在找尋和修飾有效藥物的重要方法。過去這些年關於化合物毒性的研究,也對結構和毒性之間的關係有很多的瞭解,因此不僅僅在藥物的合成上必須嚴謹,對於功能性的化學產品,例如油漆、黏著劑、染料、塑化劑等等,也應依循此原則來設計,減少對人體和環境的危害。
降輔(V)
在一個化學反應或製程裡,常需要運用一些輔助性的物質,例如溶劑,或分離純化產物所用的化學材料,這些化學物質雖然不會出現在產物的結構之中,但是使用它們時,對於環境的影響也必須考慮,因此本原則的重要精神,就在於可能的話,盡量少用這些輔助性的材料。
上述透過圖1的例子,介紹了原子效率來對化學反應進行理論上的評估,但是為了看清整個實際執行過程的效率,謝爾頓(Sheldon)提出了E-因子(E-factor)來估算:
E-factor=副產物的公斤數/產物的公斤數
上式中的副產物,包括了廢棄物以及溶劑的損失,產物的量是指真正得到的值。E-因子愈大,代表效率愈差。如果廢棄物以及溶劑能盡量回收再利用,E-因子就可降低。一個負責任的化學工廠,應該很清楚的知道它的化學製程所具有的E-因子,而且應以達到E-因子為零的理想目標來調整。從表1提供的各化學產業概況,可以看到雖然石油精煉產業的E-因子很低,但是由於其巨大的規模,廢棄物淨值仍然是極為龐大的,若能減少千分之一,就等同於製藥業一年所產生的,因此是更需要努力的。
表1 一些化學產業的E-因子
|
產業
|
年產量(噸)
|
E-因子
|
廢棄物淨值(噸)
|
|
石油精煉
|
106-108
|
約0.1
|
106
|
|
大宗化學原料
|
104-106
|
小於1-5
|
105
|
|
精密化學品
|
102-104
|
5-50
|
104
|
|
藥物
|
10-103
|
25-100
|
103
|
在降輔的精神下,溶劑的使用是最值得下手改進的部分。理想上最好是不用溶劑,然而這並不容易。反應的所有試劑不見得一定互溶形成均勻相;而非均勻相的反應,因為發生在介面,反應速率不易掌握,複製率降低。即使是均勻相,若不使用溶劑,黏稠度常偏高,不易攪拌。針對這幾個問題,溶劑可讓反應在均勻相進行,且降低黏稠度以促進攪拌。對於放熱的反應,若不使用溶劑,熱量不易散失,易導致溫度不易控制,這尤其在大量的製備時特別危險;溶劑則可扮演吸收熱能的角色,而且反應溫度不會超過溶劑的沸點,易於控制溫度。不同溶劑,極性不同,適當的溶劑可增進反應速率。即便溶劑無法廢去,減量絕對是應該考慮的,而且要選擇對人體和環境無害的。
溶劑的第一選擇就是用水,然而眾多的有機化合物對水的溶解度很低,這使得化學家經常需要使用揮發性的有機溶劑。溶劑的揮發性,是為了方便去除,但容易逸散到大氣中造成污染。因此近幾十年來,如何取代揮發性的有機溶劑,而改用對環境影響小或低揮發但可回收的溶劑,成為重要的研究方向。在此簡單的介紹兩種作法,一個是超臨界的二氧化碳,另一個是離子液體。
我們都知道液體加熱超過沸點就成為氣體,在沸點時是液相與氣相兩相可共存的狀態,而二者的介面有很明確的區隔。但是當壓力高過某一數值時,液體受熱會找不到沸點,此壓力稱為臨界壓力。另外在固定的溫度時,外界壓力升高時,氣相會在某一壓力突然變成液相。但是當溫度超過某一數值時,壓力再怎麼升高,都找不到氣體突然變成液體的那一點,這個溫度被稱為臨界溫度。當物質處在超過臨界壓力和溫度時的狀態,被稱為超臨界流體。超臨界流體的特質是其溶解能力類似液體,但是滲透性又趨近於氣體。許多常見物質的臨界壓力和溫度偏高,但是二氧化碳很獨特,它的臨界點發生在72.8 atm 和 31 oC,不需要昂貴的儀器即可產生超臨界二氧化碳。超臨界二氧化碳的極性低,溶解能力近似於有機溶劑,而且可以透過壓力的改變調控溶解度,去除不但容易,又因為來自於環境,回到環境不會造成污染。其最著名的使用,就是咖啡因的萃取,工業界仍須多加利用它的特質。
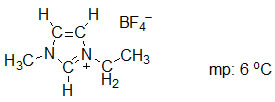
圖4 所示之[emim]BF4是一個離子化合物,但是熔點低,在室溫為液體
另一個值得注意的就是離子液體(圖4),通常離子類的化合物都是固體,但是有一類型的離子化合物卻具有很低的熔點,有的甚至於在常溫也是液體,它們在結構上通常具有一個結構巨大的有機陽離子,對於很多的有機化合物,具有很好的溶解度。離子液體的特點是揮發性低,不會逸散到環境中,也容易回收再使用;但要將有機產物取出,仍須用有機溶劑萃取,此外其毒性仍待仔細的研究。
節能(T)
化學反應的能量需求,應做仔細評估和設計,理想的反應條件是能在常溫及常壓下執行。由於催化劑可以讓反應在較低的溫度下進行,是節能最佳的選擇。近年來發現有些反應可以利用微波或超音波來加速,也是一個節能可以走的方向。我們不能忽略,能量的浪費就是資源的浪費,也會增加對環境的污染。
再生(R)
物料的來源需要從可再生的方向來努力,目前有機化合物的合成,追溯其起始物,大部分來自石油裂煉的產物,石油這樣的資源是在短期內無法再生的,這對地球資源的浪費是很可怕的。理想的作法是從動植物的來源取得原料,現在有許多化學家投入這個領域,開發新的而且更有效的方法。但這領域面臨了人類對糧食需求的壓力,培育植物對土地面積的需求,以及再製過程中能量的耗費等等的問題,這些困難需要新的技術來克服。
植物天生的知道如何將二氧化碳轉變成為有機化合物,化學家需要向植物學習,研發更有效的方法,把二氧化碳變成再生的物料,作為碳的來源,同時還可達到減少溫室效應的效果。
我們也需要開發好的方法,將廢棄的化學產品回收,轉換成有用的資源,而非直接燒掉變成二氧化碳。例如有科學家正在開發方法,將垃圾中的有機物轉換成一氧化碳和氫氣,這正是所謂的合成煤氣(syngas),既可當成能源轉換成電能,亦可透過合成方法,將之轉換成高碳數的油料;此外無機金屬的部分,可另外回收再利用。
簡潔(O)
有機化合物的合成,倚賴官能基的轉換。為了提升某官能基的活性,常需要將之轉成另一個活性較高的官能基,完成任務後再恢復原樣。有些時候這樣做,是為了降低某官能基的活性,避免它參與不必要的反應,有機化學家稱之為保護,在之後的某個階段,還需要去掉保護回復原狀。這些轉換都需要額外的試劑、操作、和能量的消耗,我們應對此仔細評估和研究,發展新的合成方法,減少不必要的步驟。
催化(C)
催化劑可降低反應活化能,使得反應速率加快,因此能在較溫和的條件下進行化學反應。它不會變成產物結構的一部份,只扮演幫助的角色,當一個產物分子生成後,它就功成身退,重新開始另一輪的催化;因為這個循環的特質,所以不需要用很多。在工業上,理想的催化劑用量希望少於0.01當量,意思就是說一莫耳的反應物,只需要用0.01莫耳的催化劑,好的催化劑甚至於只要用0.001當量就可以。
前述的說明,已經多次的提到催化劑的好處,總括來說,它具有減廢、提高效率、和節能等好處,因此我們應該儘可能的使用催化的方法。更進一步的,我們應該研發更多可回收再使用的催化劑,例如使用固體的酸或鹼,不但透過過濾或離心即可回收,亦省去反應完畢中和酸鹼然後產生很多鹽類廢棄物的問題。此外固體的物質,運送和使用也很方便安全。
近幾十年,生物催化劑的使用和研發受到重視。透過演化,大自然在生物的體系內創造了許許多多非常有效率的催化劑,我們常稱這些生物催化劑為“酶”。它們的高效率,使得重要的生命化學,可以在常壓和常溫迅速的進行。它們各自扮演不同的功能,例如有的進行酯的水解或合成(酯酶);有的進行還原 (還原酶);有的可以進行醯胺的水解或合成(醯胺酶)。我們可以直接透過細胞,或是分離純化出酶,來幫助化學家進行反應。大家熟知的,就是利用酵母菌來分解糖得到酒精。
拜基因工程近幾十年的快速發展所賜,化學家已經能夠修改某些基因,讓細胞從二氧化碳合成出某些小分子的有機化合物,做為燃料,或者做為合成更複雜化合物的原料。可預見的未來,我們不需要透過石油來取得有機化合物的原料。合成的有機物質,透過代謝或燃燒,最後轉成二氧化碳,再從二氧化碳透過細胞或生物催化劑製造原料或燃料,完美的生成一個永續的再生循環,這正是人類應該向大自然學習的功課。
可解(D)
為了完成上述永續的再生循環,我們所創造的有機化合物,必須能在自然環境中分解成無害的化合物而不累積。眾所周知的就是聚乙烯這類的塑膠,因為無法分解,一旦棄置就造成很大的環境壓力。長此以往,地球將成為很多人看過的那部電影“瓦力”裡面描繪的樣子。因此化學家有責任,在一開始設計的時候就以能分解為原則。再一度的,在大自然裡面存在的許多結構單元,是我們設計的範本,因為大自然裡有一套方法,針對這些結構來代謝。
對於這個原則而言,一個最著名的例子就是有關清潔劑的發展。由於肥皂易與硬水中的鎂、鈣等金屬離子生成不溶於水的固體,因此發展了TPBS (tetrapropylene benzene sulfonate) (圖5) 做為清潔劑,因為磺酸鹽在水中的溶解度很好,解決了上述產生固體污垢的問題。然而在污水處理廠的分解槽中,TPBS只能達到50%的分解,而其產生的泡沫過多,甚至逸出槽端,使得槽端工作步道濕滑,而有員工滑落窒息而亡,流到河川中造成的泡沫亦影響生物的生存。當時測試河水,其中的TPBS可高達每公升2毫克,甚至於自來水龍頭流出的水也會產生泡沫。
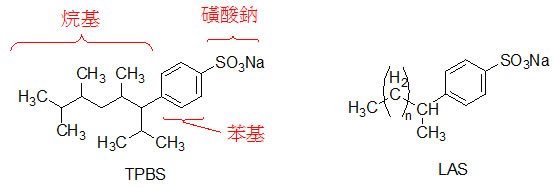
圖5 兩種清潔劑TPBS與LAS的結構,前者的烷基分岔過多,不易代謝,後者則無此問題
TPBS不易代謝是由於苯環上的烷基分岔過多造成,生命體系製造的油脂類化合物,結構上攜帶的都是直鏈型的脂肪酸,有天然的酶可將之分解,但是分岔過多的烷基與生物體系存在的結構差異大,就不易分解了。瞭解了這個原因後就發展出了LAS (linear alkyl benzene sulfonate),其結構中的烷基是線型的,容易代謝,也就解決了問題。美國在1960年代,TPBS就被LAS完全取代了。
現在對生物體系的瞭解已經超越60年代太多,以化學家擁有的能力,應採取預防重於治療的態度,從設計面開始才是最好的永續之道。
監測(I)
基於「你無法控制無法測量的物質」的概念,化學家需要發展分析的方法,及時以及當場的監測毒性物質產生狀況,這樣才能配合操作,立即調整反應條件,消除毒性物的出現。及時監測也讓我們能夠精準的知道反應試劑消耗的狀況,避免材料的浪費;也可以掌握反應結束的時間,避免反應時間過長,造成副產物的增加以及能量的浪費。
思危(Y)
化學安全的考量必須是全面性的,而不是僅聚焦在防止污染,和對環境的影響。整個化學製程的試劑,牽涉的毒性、爆炸性、和易燃性,都應該從設計面來處理。例如整個製程若會產生具有毒性的過渡物質時,就應考慮在反應爐中當即產生當即轉換的作法,以避免危險化學物質的處理和大量的存放。
我們應該聽過太多工廠的事故,不但造成生命財產的損失,環境的破壞,事故造成民眾對化學的反感,是更難修補的。
結語
化學的運作是與生命的存續息息相關的,也是地球的命脈所繫,我們應該尊重它,瞭解它,而不是畏懼它,糟蹋它。我們的目光不應侷限在目前,而需思考未來,但是未來是建築在目前的作為上,未來的地球究竟是享受我們帶給它的幸福,還是詛咒我們為它帶來的苦果,決定權是在現今的我們。要民眾對化學重視而不抗拒,有賴於化學家保有一顆關懷永續的心,建立大眾對化學的信心。綠色化學需要新的觀念,新的作法,和新的工作者加入,讓我們為拯救地球的未來而努力。
註
Tang、Smith 和 Poliakoff提出的 ”PRODUCTIVELY” 這十二個英文字母對應的英文原意如下:
P: Prevent wastes (對應於防廢)
R: Renewable materials (對應於再生)
O: Omit derivatization steps (對應於簡潔)
D: Degradable chemical products (對應於可解)
U: Use safe synthetic methods (對應於保安)
C: Catalytic reagents (對應於催化)
T: Temperature, Pressure ambient (對應於節能)
I: In-Process Monitoring (對應於監測)
V: Very few auxiliary substances (對應於降輔)
E: E-factor, maximize feed in product (對應於物盡)
L: Low toxicity of chemical products (對應於低毒)
Y: Yes, it’s safe (對應於思危)
參考資料
- Anastas, P. T.; Warner, J. C. Green Chemistry: Theory and Practice; Oxford, 2000.
- Lancaster, M. Green Chemistry: An Introductory Text; RSC, 2002.
- Matlack, A. S. Introduction To Green Chemistry, 2nd Ed.; CRC, 2010.
- Ahluwalia, V. K. Green Chemistry, 2nd Ed.; CRC, 2012.
- Xie, H.; Gathergood, N., Eds. The Role of Green Chemistry In Biomass Processing And Conversion; Wiley, 2013.
- DeVito, S. C.; Garrett, R. L., Eds. Designing Safer Chemicals; ACS, 1996.
- Sheldon, R. A.; Arends, I; Hanefeld, U. Green Chemistry and Catalysis; Wiley-VCH, 2007.
- Cann, M. C.; Connelly, M. C. Real-World Cases in Green Chemistry; ACS, 2000.
附記
本文的目的,在企圖為高中化學以及科普教育推薦一個極端重要的觀念。我希望高中老師讀過了之後,能在化學教育中植入這個想法,讓它有萌芽的機會;高中學生讀過之後,能瞭解化學這些年來重要的走向,或許能夠心動而加入化學家的行列;大學裡和化學相關科系的學生讀過之後,能常保此十二原則於心;普通民眾讀過後,能理解化學的重要性,支持永續化學的作法。化學不應是麻煩的製造者,而是幸福的來源。我的前輩老師,國立臺灣大學化學系的劉廣定教授,多年來致力於國內永續化學觀念的推廣,曾多次叮囑筆者,應想辦法將這個概念融入教學,筆者一直未能做到,含愧至今,因此本文實有彌補缺憾之意。